“Stefano” e “Nefasto”.
Il primo è il nome di chi vi scrive, il secondo ne è l’anagramma: una parola costituita dalle stesse lettere della prima, ma messe in un ordine diverso. Come potete notare a seconda di come le lettere vengono ordinate, il risultato può essere profondamente diverso: da un nome di persona si ottiene un aggettivo, nemmeno tanto (ahimè) di buon auspicio.
Analogamente è possibile utilizzare gli stessi elementi per formare molecole organiche diverse; questi manterranno stessa formula bruta, ma diversa disposizione. Due molecole con queste caratteristiche sono chiamati isomeri.
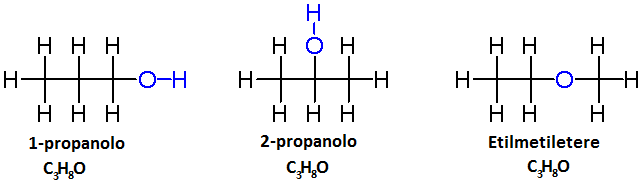
Due isomeri possono essere anche molecole molto diverse fra loro, con caratteristiche chimico-fisiche ben distinte: per esempio la molecola con formula bruta C3H8O può essere considerata come un alcol (anzi due alcoli diversi) o anche come un etere, a seconda di come i suoi atomi si dispongono.
Le modalità in cui l’isomeria si manifesta sono diverse e dipendono, quindi, dal modo in cui gli atomi sono disposti nello spazio.
Nell’isomeria di catena cambia principalmente la forma della catena di atomi di carbonio. Per esempio l’esano (C6H14) possiede molti isomeri, i quali a seconda della disposizione che presentano, prendono nomi diversi, per i quali è necessario utilizzare la nomenclatura degli idrocarburi. Non sempre risulta semplice individuare due isomeri di catena, scriverne la formula bruta è un buon metodo per accorgersene.

L’isomeria di posizione, invece, consiste nella diversa disposizione di uno o più parti della molecola, rispetto alla catena carboniosa che funge da scheletro centrale. Per esempio in alcuni alcoli, è necessario indicare il numero dell’atomo di carbonio al quale il gruppo ossidrilico (-OH) è legato, proprio in modo da distinguere i vari isomeri, come nel caso del pentanolo (C5H12).

In maniera simile, due isomeri di posizione possono anche distinguersi per la posizione del doppio legame tra gli atomi di carbonio, nel caso di idrocarburi insaturi.

Il 2-pentene (a destra) in realtà può trovarsi in due forme alternative, in cui la disposizione spaziale dei sostituenti rispetto al doppio legame cambia. In questo caso parliamo di stereoisomeria, che per i doppi legami carbonio-carbonio, assume una nomenclatura particolare: si utilizza il termine trans per indicare l’isomero in cui i sostituenti si trovano opposta fra loro rispetto al doppio legame, mentre cis nel caso in cui si trovano dalla stessa parte.

Un altro particolare tipo di stereoisomeria è l’isomeria ottica, in cui due molecole si distinguono per come i sostituenti legati a un atomo di carbonio sono disposti nello spazio, nel caso in cui ci siano 4 sostituenti diversi. Se i due stereoisomeri sono l’uno l’immagine speculare dell’altro parliamo di enantiomeri. Le nostre mani sono un esempio classico di come due oggetti presentano proprietà tali per cui possiedono un'immagine speculare non sovrapponibile a sé. Il carbonio che lega i quattro sostituenti viene definito comunemente chirale, o anche elemento stereogenico.

Coppia di enantiomeri. Nel formalismo chimico si intende il “triangolo pieno” come un legame che esce dal piano del foglio verso chi legge, mentre il “triangolo tratteggiato” come un legame che si allontana da chi legge. A, B, C e D non rappresentano elementi chimici, sono solo lettere di esempio.
Credits: Wikimedia Commons V8rik