Il gioco del superenalotto consiste nell’indovinare una combinazione di sei numeri che vanno dall’1 al 90. Chiunque almeno una volta nella vita avrà pensato alla possibilità di puntare su tutte le combinazioni esistenti per avere la certezza della vittoria, per poi rendersi immediatamente conto che esse sono talmente tante (oltre 622 milioni) che la cifra così vinta sarebbe di gran lunga inferiore al costo della schedina. Allo stesso modo la grandissima varietà di molecole esistenti permette di pensare a un numero elevatissimo di diverse reazioni, che porteranno a prodotti differenti.
Ricordiamo che una reazione chimica è una trasformazione che comporta una nuova distribuzione degli atomi in una o più determinate specie di materia, senza misurabili variazioni di massa.
In una reazione abbiamo quindi i reagenti, sostanze “di partenza” e i prodotti, sostanze “d’arrivo” in cui i reagenti si trasformano.
Un modo per classificare i vari tipi di reazione si basa sul meccanismo con cui le molecole interagiscono tra loro.
Alcuni esempi:
Reazione di sintesi
A + B → C
Questo tipo di reazione permette di ottenere un singolo prodotto a partire da due o più reagenti:
Es.
4 S8 (s ) + 4 O2 (g ) → 4 SO2 (g )
H2 (g ) + Cl2 (g ) → 2 HCl (g )
Reazione di decomposizione
AB → A + B
In questo tipo di reazione, detta anche analisi, inversa alla precedente, una molecola può essere divisa in due o più specie.
CaCO3 (s ) → CaO (s ) + CO2 (g )
2 AgCl (s ) → 2 Ag (s ) + Cl2 (g )
Reazione di scambio semplice o sostituzione semplice
AB + C → AC + B
In questo tipo di reazione una specie costituita da un solo elemento è in grado di sostituirsi a uno o più atomi presenti in un altro composto. In questo modo si formano due nuove molecole, che spesso hanno caratteristiche profondamente diverse da quelle dei reagenti.
2 Mg (s ) + SiO2 (s ) → 2 MgO (s ) + Si (s )
Talvolta le reazioni di scambio semplice coinvolgono ioni disciolti in soluzioni acquose, definiti "acquoioni" (aq).
Zn (s ) + 2 HCl (aq ) → ZnCl2 (aq ) + H2 (g )
Reazione di doppio scambio o sostituzione doppia
AB + CD → AC + BD
Come suggerisce il nome, questo tipo di reazione permette a due molecole di scambiarsi gli elementi a vicenda, andando a formare due specie distinte, diverse dai reagenti. Particolare tipo di "doppio scambio" è la reazione di neutralizzazione, in cui un acido e una base reagiscono formando un sale e acqua.
Mg(OH)2 (s ) + 2 HCl (aq ) → MgCl2 (aq ) + 2 H2O (l )
AgNO3 (aq ) + NaCl (aq ) → AgCl (s ) + NaNO3 (aq )
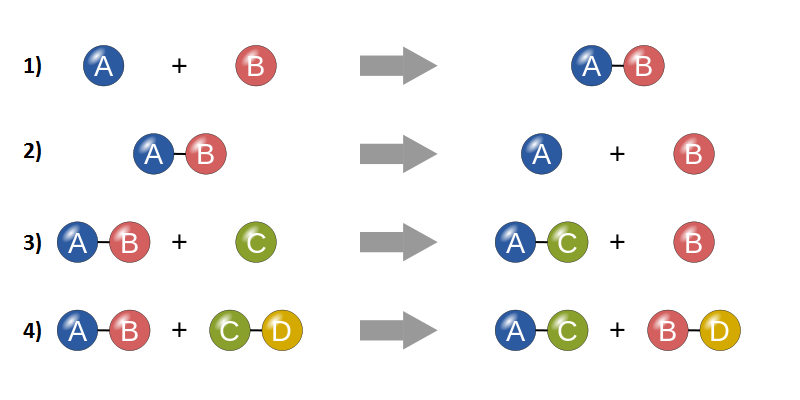
Le varie tipologie di reazione. 1) reazione di sintesi. 2) reazione di decomposizione. 3) reazione di scambio. 4) reazione di doppio scambio.
Credits: Wikimedia Commons Aushultz